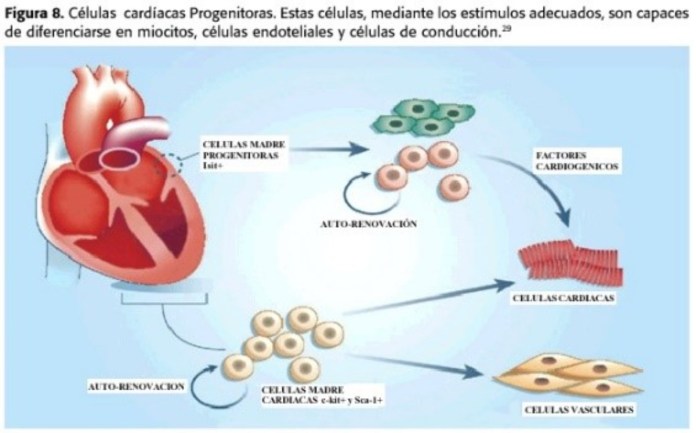
Tejido nuevo después de un infarto como tratamiento
En un ataque al corazón, millones de células del músculo cardíaco llamadas cardiomiocitos mueren debido a la reducción del flujo sanguíneo. Estos son reemplazados por tejido cicatricial fibrótico incapaces de moverse, lo que deteriora aún más la capacidad del corazón para bombear sangre por todo el cuerpo. Esto, a su vez, puede provocar insuficiencia cardíaca, una afección común y, a menudo, mortal que afecta a más de 60 millones de personas en todo el mundo.
Un nuevo tipo de terapia celular puede reparar el tejido cardíaco dañado después de un infarto. Investigadores en Alemania y AstraZeneca, entre otros, han identificado un nuevo tipo de terapia celular con el potencial de curar el daño al corazón después de un ataque al corazón. El estudio preclínico, publicado en la revista Nature Cell Biology, muestra que las llamadas células progenitoras ventriculares o células madre, pueden estimular la capacidad de reparación del corazón y reducir el tejido cicatricial. Esta es la culminación de dos décadas de trabajo para encontrar la célula óptima para reparar un corazón dañado. Los resultados ofrecen una nueva esperanza para los millones de pacientes con insuficiencia cardíaca en todo el mundo que esperan un trasplante de corazón.
Esos cardiomiocitos desempeñan un papel importante en la estructura del corazón para que ese funcione bien. A diferencia del desarrollo fetal y de los niños pequeños, la capacidad del corazón adulto para formar nuevas células del músculo cardíaco es muy limitada. Por ello, muchos investigadores están interesados en la posibilidad de utilizar la terapia celular para estimular la capacidad regenerativa del corazón. Los estudios anteriores se habían estado centrado en parte en los cardiomiocitos maduros, pero los efectos secundarios, como los trastornos del ritmo cardíaco, han impedido hasta ahora el uso clínico.
El estudio actual examinó las llamadas células progenitoras ventriculares humanas (HVP, por sus siglas en inglés), que son células inmaduras del músculo cardíaco y desempeñan un papel importante en la estructura del corazón durante el desarrollo fetal. Los investigadores cultivaron y purificaron miles de millones de estas células HVP a partir de células madre embrionarias humanas. Posteriormente, se examinó la capacidad de las células para reconstruir la función del músculo cardíaco en una cámara de cultivo celular tridimensional y en cerdos con daño cardíaco.
Afirman los investigadores que en su trabajo en sus laboratorios vieron cómo las células HVP migraban a las regiones dañadas del corazón donde luego maduraban hasta convertirse en células cardíacas sanas que funcionaban y contrarrestaron la formación de tejido cicatricial ocupan bien su lugar. Los resultados representan un hito importante en el trabajo de encontrar un posible tratamiento con células HVP para pacientes con insuficiencia cardiaca severa, especialmente para edades en las que la cirugía cardiaca implicaría mucho estrés, dicen los autores-
Luego del trabajo en laboratorio, los investigadores se lanzaron a estudios con animales y observaron una clara mejora en la función cardíaca en cerdos inyectados con células HVP después de una lesión en comparación con el grupo no tratado. Los cerdos fueron observados para ver si se producían otras anomalías y durante el período de seguimiento de tres meses, no se observó formación de tumores, lo que es prometedor para cualquier estudio clínico futuro.
Así que, por el momento, los resultados apuntan a una capacidad única de las células HVP para regenerar el tejido cardíaco, reducir el tejido cicatricial y mejorar la función cardíaca en cerdos con insuficiencia cardíaca isquémica sin producir la temible complicación de tumores. Así que a la vista tenemos alentadamente la posibilidad de una nueva terapia basada en células HVP y la oportunidad de encontrar otros nuevos usos en el futuro en tratamientos cardiovasculares para contrarrestar las lesiones por insuficiencia cardíaca y desarrollo temprano en el campo de enfermedades cardiovasculares, renales y metabólicas.
En un próximo paso, los investigadores planean realizar, entre otras cosas, estudios toxicológicos e investigar la posibilidad de desarrollar líneas celulares que sean toleradas por el sistema inmunitario. En la actualidad, se requiere tratamiento con fármacos inmunosupresores para evitar que el sistema inmunitario rechace las células HVP trasplantadas. La esperanza es comenzar los ensayos clínicos dentro de los próximos dos años. Que surte la de las nuevas generaciones.
Vacuna y corazón
Un problema actualizado, hablando de corazón está en la mente de todos: Miocarditis (inflamación del corazón) como efecto secundario raro después vacunación con ARNm y vale la duda.
El aumento de la incidencia de miocarditis, especialmente en hombres jóvenes que han sido vacunados con una de las vacunas de ARNm, se ha confirmado. El riesgo de infarto de miocardio, pero hasta la fecha, la aparición de miocarditis y pericarditis después de la vacunación ha sido muy rara. La miocarditis y la pericarditis eran efectos secundarios que, en casos muy raros, pueden ocurrir después de la vacunación, con riesgo mayor después de la segunda dosis, el riesgo de miocarditis dentro de los 28 días posteriores a la vacunación fue mayor después de la segunda dosis que después de la primera y más alto para los hombres jóvenes, en comparación con los hombres de 16 a 24 años no vacunados, se habla de entre 3-7 casos adicionales de miocarditis por cada 100 mil vacunados. La mayoría de las miocarditis ocurrieron dentro de los primeros 7 a 10 días después de la vacunación. Aún más raro y extraño es que se produjeran muertes entre los menores de 40 años que padecían miocarditis.
La miocarditis entonces es rara y se necesita una población de millones, más grande para poder estudiar estas conexiones y en la actualidad se suman datos de varios países con resultados preliminares y un trabajo de análisis continuo para estudiar con más detalle estos riesgos y conexiones, así como el pronóstico de los afectados. Usted por el momento tranquilo, la incidencia de miocarditis y pericarditis después de la vacunación es muy rara, y los beneficios de estas vacunas para reducir el riesgo de enfermedad grave por Covid-19 y muerte superan los riesgos de efectos secundarios como este.
Vacuna contra COVID-19 y enfermedad autoinmune
Y a propósito la vacuna en pacientes con enfermedad autoinmune como esclerosis múltiple, la vacuna se ha dicho que no pega también. En muchos países, el rituximab es el medicamento más común para la esclerosis múltiple (EM), pero también se usa para muchas otras enfermedades y lo que se ha encontrado es que los pacientes con EM tratados con rituximab tienen un mejor efecto de la vacuna Covid-19 si el nivel de células B es más alto. En pacientes con células B de 40 / μL (microlitros) o más, 9 de cada 10 pacientes desarrollaron un nivel protector de anticuerpos, mientras que hubo una cantidad significativamente menor entre aquellos con niveles más bajos. Anteriormente se suponía que bastaba con esperar cierto tiempo tras el tratamiento con rituximab para que la vacuna surtiera un buen efecto. Pero para aumentar la posibilidad de que la vacuna provoque que el cuerpo forme anticuerpos, primero debe medir el nivel de células B y asegurarse de que sean lo suficientemente numerosas, dicen los que ha estudiado esto
El tratamiento con rituximab y tiene un buen efecto documentado cuando se trata de ralentizar la EM. El tratamiento elimina las células B del cuerpo, que son una parte importante de nuestra respuesta inmunitaria, pero que también contribuyen al proceso de la enfermedad en la EM. El paciente debe ser capaz de formar una cantidad suficiente de anticuerpos después de la vacunación. Cuanto más tiempo había sido tratado un paciente con rituximab, más tardan sus células B en recuperarse. Para algunos, pasa más de un año antes de que las células B comenzaran a regresar. Los pacientes con EM que nunca han sido tratados con rituximab aparentemente tienen mejor efecto con la mayor proporción de anticuerpos al vacunarse. Es entonces evidente que el tratamiento con Rituximab aumenta el riesgo de que los pacientes sufran infecciones graves, como la Covid-19.
Tener niveles bajos de células B dificulta que el cuerpo produzca anticuerpos protectores contra virus y bacterias, que es el propósito básico de las vacunas.