El aumento de la prevalencia de muchas enfermedades, se encasilla en una palabra: enfermedades autoinmunes y su desarrollo en buena parte se ha encontrado asociado con un cambio en los patrones de estilo de vida y dentro de este, entre otros factores, se ha señalado el aumento del consumo de ciertos componentes dietéticos como: la sal de mesa, los ácidos grasos, la ingesta calórica excesiva, la deficiencia de nutrientes como zinc, vitamina A, asociado con una tolerancia inmunológica defectuosa. Todo eso obedece a que se ha demostrado que los nutrientes de la dieta, modulan la respuesta inmunitaria, mediante un efecto directo sobre la función de las células inmunitarias o, indirectamente, actuando sobre el microbioma (composición de bacterias y gérmenes microscópicos) del tracto gastrointestinal. Otros moduladores del sistema inmunológico son medicamentos y químicos ambientales: Modular tiene dos funciones respuesta y activación que por lo general van unidos.
El sistema inmunológico está compuesto de químicos como los anticuerpos y de células. Dentro de esas células hay unas llamadas células T reguladoras que se abrevian como (Treg) suprimen las respuestas inmunitarias y son fundamentales para mantener la tolerancia periférica y la homeostasis inmunitaria, modulando la inflamación crónica de los tejidos. Ahora es bien conocido que las Treg muestran cierto grado de plasticidad (propiedad por la cual una célula puede adquirir varias identidades distintas y reversibles) para adaptar su función reguladora inmune a diferentes situaciones fisiológicas durante una respuesta inmune. Sin embargo, en la actualidad no se comprende bien qué señales ambientales regulan la plasticidad y función de Treg, pero eso será de gran importancia para fines terapéuticos.
Primero que nada debemos tener claro que el comportamiento del sistema inmune ante agresiones internas y externas sobre células tejidos y órganos del cuerpo, funciona buscando un equilibrio apropiado entre las respuestas inmunes proinflamatorias y antiinflamatorias para proteger a los componentes orgánicos mencionados, que pueden ser afectados por patógenos invasores e internamente contra el desarrollo de tumores, sin que todo ese trabajo permita caer en enfermedades autoinmunes y alérgicas. Eso es en teoría lo que se espera de un buen sistema inmune.
Entonces, si bien se han identificado diferentes poblaciones de células con actividad antiinflamatoria, las células T reguladoras CD4, FOXP3 (Tregs) son las mejor definidas. El factor de transcripción FOXP3 determina el linaje de las células Treg y es esencial para una homeostasis inmunitaria adecuada. FOXP3 tiene gran importancia pues ha sido definido por diversos autores como el gen maestro controlador del desarrollo y función de las células reguladoras. Las mutaciones de pérdida de función en foxp3 conducen a trastornos inmunes fatales en humanos.
Las Treg trabajan suprimiendo las respuestas inmunitarias innatas y adaptativas utilizando una amplia gama de mecanismos moleculares que, por ejemplo, involucran mecanismos dependientes del contacto celular, la liberación de factores solubles (son elementos bioactivos, de naturaleza proteica. Son sintetizados por diferentes tipos celulares y actúan como comunicadores químicos entre células y tejidos), la privación de factores de crecimiento (son proteínas que hay en la sangre y que tienen como función la comunicación intercelular para reparar lesiones), la inducción de apoptosis (proceso de muerte celular programada) de células diana e hidrólisis (liberación de energía) de ATP y producción de adenosina.
Aunque existe versatilidad en la respuesta de Treg que permite una respuesta especializada según el entorno, la ubicación anatómica y el tipo de célula a suprimir, la evidencia creciente sugiere la falta de estabilidad de Treg como culpable de la autoinmunidad. Las Treg aisladas, por ejemplo, de pacientes con diabetes Tipo 1, EM y LES mostraron la adquisición de funciones pro inflamatorias y una potencia supresora reducida in vitro.
Decíamos arriba que los patrones de estilo de vida occidentales, son importantes desencadenantes de la enfermedad. Se ha propuesto una variedad de factores para favorecer el desarrollo autoinmune, como la disminución de la exposición a patógenos, el humo, las hormonas, el estrés, los contaminantes, los componentes de la dieta y la obesidad. Además, cada vez hay más datos que destacan la compleja interacción entre la nutrición, el estado metabólico y la respuesta inmunitaria.
La restricción calórica (no confundir con deficiencia) disminuye la gravedad de la enfermedad y aumenta la vida útil en modelos animales experimentales de inflamación y autoinmunidad. Por el contrario, la obesidad es uno de los factores más consistentes que predisponen a la autoinmunidad, al estar relacionada con esclerosis múltiple, psoriasis y enfermedad de Chron entre otras. Además, la dieta altera la composición microbiana intestinal. Las bacterias intestinales y sus metabolitos regulan las respuestas proinflamatorias y reguladoras de las células T en el intestino, lo que podría ejercer efectos sistémicos en el individuo como se ejemplifica en el siguiente gráfico
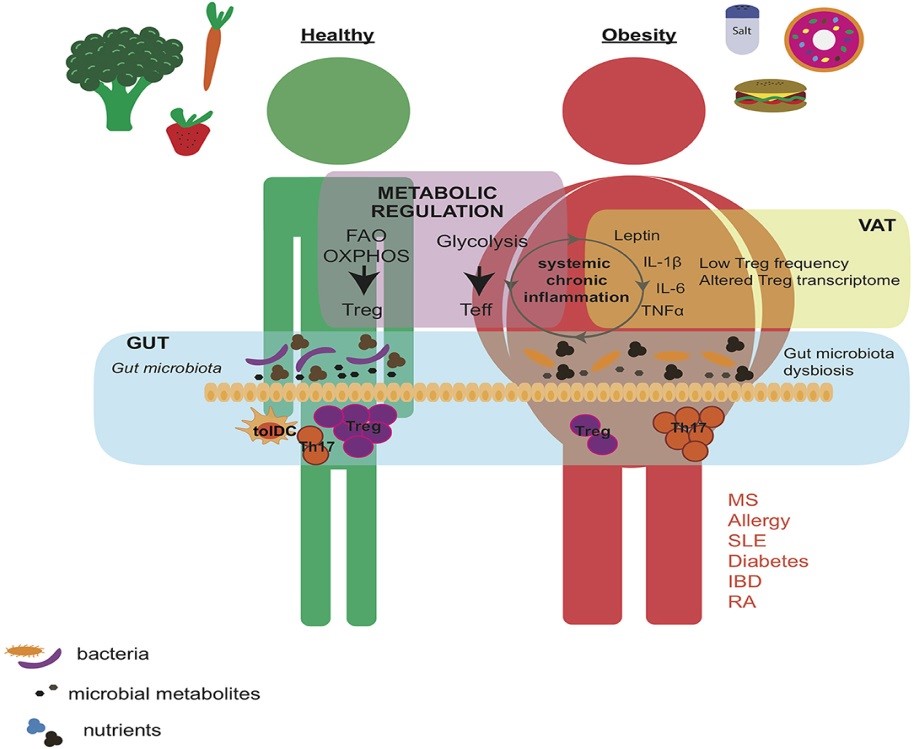
Es indudable, como se muestra en la figura, que una mala dieta afecta la composición microbiana intestinal e induce una inflamación crónica de bajo grado que altera el estado metabólico del individuo. Una dieta saludable, apoya el crecimiento de especies bacterianas que, mediante la producción de metabolitos inmunomoduladores (son moléculas de origen sintético o natural que regulan o modulan la respuesta del sistema inmune según las necesidades de cada organismo), promueve la inducción de Treg sobre el desarrollo de células Th17 en el intestino. Por el contrario, la dieta caracterizada por una alta ingesta calórica y altos niveles de sal y colesterol, conduce a la obesidad, aumenta la secreción de adipocinas y citocinas proinflamatorias y altera la composición microbiana intestinal. Es importante destacar que las células Treg y Teff desarrolladas en el intestino y el VAT tienen un efecto sistémico y pueden contribuir a la exacerbación de la patogenicidad autoinmune.
El tracto gastrointestinal humano, es el principal reservorio de microorganismos que incluyen bacterias y virus, todos los cuales constituyen colectivamente la microbiota comensal. Una extensa investigación ha demostrado la íntima interferencia entre la microbiota comensal y el equilibrio inmunológico. Las Treg que residen en el intestino, son fundamentales para mantener la homeostasis inmunitaria intestinal. La evidencia creciente muestra que las Treg que viven en la lámina propia del colo,n son en su mayoría inducidas periféricamente y dependen de señales derivadas de la microbiota para su correcto desarrollo y función
La frecuencia y función de las Treg, también pueden estar reguladas por vías metabólicas como la FAO, OXPHOS y la glucólisis que dependen del estado nutricional del individuo. El metabolismo celular regula el desarrollo celular y su proliferación y función, y es controlada por señales ambientales y la disponibilidad de nutrientes. Las vitaminas y los índoles (compuestos nitrogenados que se encuentran en la col y en otros vegetales crucíferos) también modulan la función Treg.
¿Qué tiene que ver la obesidad con lo inmune se preguntará? pues claro que tiene que ver. Las calorías excesivas se almacenan como grasa en el tejido adiposo, que también actúa como un «órgano endocrino» liberando adipocinas proinflamatorias y citocinas, lo que propicia el aparecimiento de enfermedades crónicas sistémicas. Múltiples tipos de células inmunes, residen en el tejido adiposo y juegan un papel en la inflamación y la desregulación metabólica.
Las hormonas también tienen su rol. La leptina favorece las respuestas Th1 y la diferenciación Th17, pero inhibe la proliferación de Treg. Además, los ratones deficientes en leptina muestran disminución de la inflamación patógena en la mayoría de los modelos experimentales de EII, AR y EM.
¿Y la sal? El aumento de la ingesta de sal, que también es común en muchas dietas, se ha relacionado con la enfermedad cardiovascular y la autoinmunidad.
En resumen: Además de los factores genéticos, se cree ampliamente que la dieta occidental, caracterizada por una alta ingesta calórica en forma de alimentos procesados, enriquecidos en proteínas, azúcar, grasas y sal, y otros compuestos de estabilización contribuye al aumento de las enfermedades autoinmunes y otras que tiene que ver con estado inmune, en las últimas décadas.
Cada vez está más claro que la nutrición, el estado metabólico, la microbiota y la autoinmunidad, están profundamente interconectados. Además, los nutrientes de la dieta y los metabolitos microbianos alteran la respuesta inmune al actuar sobre diferentes poblaciones de células inmunes y su funcionamiento y proliferación.