Los antibióticos se usan con frecuencia para tratar enfermedades infantiles, especialmente infecciones del tracto respiratorio, otitis media y diarrea. Sin embargo, muchas de estas infecciones son virales y/o autolimitantes, por lo que no son necesarios los antibióticos. Se ha informado sobre el uso excesivo de antibióticos entre los niños en todo el mundo. En Guatemala, la prescripción excesiva de antibióticos por parte de los médicos, se ve agravada por la capacidad de comprar antibióticos sin receta médica a pesar de las regulaciones gubernamentales.
Todo producto farmacéutico acarrea sus bemoles para la salud del individuo con diferentes efectos según edad, sexo de las personas. Una gran cantidad de evidencia acumulada, ilustra el efecto perjudicial especialmente de los antibióticos en la homeostasis de la microbiota del huésped en varios sistemas, especialmente en el tubo digestivo. Los antibióticos inducen perturbaciones de la microbiota o disbiosis, lo que a su vez altera las respuestas inmunitarias del huésped contra los patógenos, con grave amenaza para la salud pública mundial
En comparación con los adultos, los tratamientos con antibióticos en lactantes, tienen consecuencias desproporcionadas, porque la microbiota infantil representa un sistema en evolución que es inestable e inmaduro hasta los 2-3 años de edad. En los últimos años, se ha vuelto evidente que los bebés, que están sujetos a frecuentes exposiciones a antibióticos debido a su vulnerabilidad a las infecciones, reflejan una mayor susceptibilidad a un amplio espectro de enfermedades, incluidas las infecciones, en la edad adulta. Relativamente menos conocimiento está disponible sobre cómo los antibióticos afectan la microbiota y la inmunidad infantil.
Qué necesitamos
Para médicos y pacientitos, conocer mejor cómo los regímenes de tratamiento con antibióticos influyen en la inmunidad innata y adaptativa del bebé e infante; cómo afecta ello la susceptibilidad a los patógenos; al igual que explicar cómo eso puede volverlos susceptibles a infecciones en la edad adulta. Respuesta que al tenerse con claridad, puede tener implicaciones para el desarrollo de nuevos tratamientos efectivos contra enfermedades y alterar la susceptibilidad a infecciones en su vida actual y posterior.
Qué sabemos
Hasta hace poco, todavía se creía que era posible que los bebés estaban expuestos a la microbiota materna y sus metabolitos que atraviesan la placenta y entran al líquido amniótico y tejidos fetales. Pero ahora que se sabe que los tejidos fetales y placentarios son estériles la mayor parte del embarazo y que alrededor de la época del trabajo de parto y el nacimiento, se produce una importante transferencia y colonización de microbiota intergeneracional, que continúa hasta los 3 años de edad. Esto se cree que contribuye al desarrollo y la educación del sistema inmunitario de los recién nacidos, a menudo denominado impronta inmunológica, que los prepara para responder de manera óptima a las «señales de peligro» en fases posteriores de la vida. De ser así, las perturbaciones compositivas y funcionales de la microbiota que son posibles, generalmente se denomina disbiosis, que puede tener consecuencias desproporcionadas en esta etapa. Esas dos posiciones (vida fetal o inmediatamente antes del nacimiento y después del mismo) permanecen contradictorias y motivo aun de discusiones.
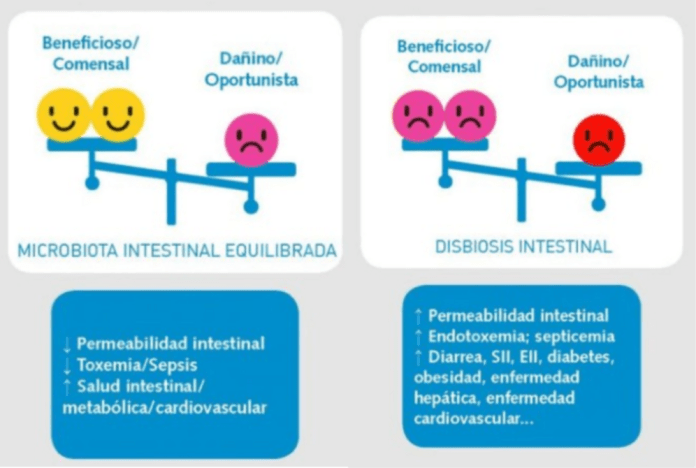
Los factores importantes que causan la disbiosis incluyen, pero no se limitan a, los hábitos dietéticos, el estrés, el tipo de parto (cesárea o vaginal) y los antibióticos. La disbiosis provocada por antibióticos, en particular, se erige como un fenómeno importante, clínicamente relevante, que se correlaciona con una gran cantidad de enfermedades. Por lo general, conduce a una disminución de la diversidad microbiana tanto en niños como en adultos, aunque la naturaleza de los efectos depende de múltiples factores, como los tipos y las dosis de antibióticos. Los efectos de los antibióticos sobre la microbiota pueden durar más allá de la infancia y tener consecuencias a largo plazo para la salud y la enfermedad. Por ejemplo, estudios retrospectivos de casos y controles, han encontrado que la exposición prolongada a la terapia con antibióticos se asocia con un mayor riesgo de enterocolitis necrosante, sepsis de aparición tardía o muerte entre los bebés de muy bajo peso al nacer. Al analizar la microbiota y los metabolitos de las heces de los bebés prematuros con siete días de tratamiento antibiótico empírico, se ha demostrado una reducción significativa en la diversidad bacteriana y el enriquecimiento de patógenos, como Streptococcus y Pseudomonas. Otros estudios hablan de que los antibióticos maternos prescritos antes o durante el embarazo, se asocian con un mayor riesgo de hospitalización infantil relacionada con infecciones. Aunque estos estudios brindan indicaciones cruciales sobre una mayor susceptibilidad a la infección. Curiosamente, en condiciones ambientales totalmente asépticas (higiene total), los animales que no fueron expuestos a antibióticos, revelaron una mayor susceptibilidad a la infección por el virus que se usaban en la exposición. Esto subraya la necesidad de estudiar mejor relación entre las condiciones higiénicas en las que se crían los niños y el desarrollo de la inmunidad contra las infecciones.
Entonces hasta la fecha, los estudios enseñan que los antibióticos perturban significativamente la composición de la microbiota, lo que conduce a consecuencias duraderas en la susceptibilidad del huésped a las infecciones virales y bacterianas. No cabe duda que la disbiosis impulsada por antibióticos, imparte un profundo impacto en la generación de respuestas inmunitarias innatas y adaptativas del lactante frente a patógenos y vacunas e influye en las células inmunitarias innatas, como las células dendríticas (DC), las células asesinas naturales (NK) y las células linfoides innatas. Pero aún no se comprende bien cómo altera la disbiosis la función de las células B y T. Podría ser que la disbiosis provoque una producción alterada de metabolitos, como los ácidos grasos de cadena corta, por bacterias comensales, que desempeñan un papel clave en la generación de células T reguladoras pero no se comprende bien el efecto en inmunidad adquirida en general.
Resumen:
Los antibióticos son a menudo un fármaco ineludible de la atención clínica para prevenir y tratar las infecciones bacterianas.
Las infecciones bacterianas imponen una carga socioeconómica considerable a la sociedad. Esto se debe principalmente a muchas condiciones que involucran al sistema de salud y al paciente pero con consecuencias en ambos. En el caso del sistema de salud, cada vez hay más conciencia sobre las graves consecuencias del uso de antibióticos en los lactantes, en niños y a todas las edades. Los antibióticos promueven cambios en la ecología microbiana, que se han implicado en respuestas inmunitarias alteradas contra patógenos y una mayor susceptibilidad a infecciones en etapas posteriores de la vida.
Comprender cómo los tratamientos con antibióticos durante la infancia da forma a la microbiota y la inmunidad es crucial, para diseñar mejores estrategias profilácticas y terapéuticas.
No está claro como los antibióticos pueden modular directamente la función inmunitaria infantil y escolar y los estudios futuros deben abordar las siguientes preguntas: 1. ¿Cuáles son los mecanismos subyacentes mediante los cuales la disbiosis provocada por antibióticos controla las respuestas inmunitarias a las vacunas y las infecciones? 2. ¿Actúan los antibióticos directamente sobre el sistema inmunológico sin involucrar a la microbiota? 3. De existir ¿Cómo se pueden neutralizar los efectos negativos del uso de antibióticos para fortalecer los programas de administración de antibióticos? 4. ¿Cómo desarrollar modelos en humanos para estudiar el efecto antibiótico sobre la microbiota y la inmunidad?
A menudo, la razón principal que se da para restringir el uso de antibióticos es retrasar el desarrollo de la resistencia a los antimicrobianos. Sin embargo, la evidencia reciente ha sugerido que los antibióticos también pueden tener un impacto negativo directo en los pacientes a los que se prescriben los medicamentos, principalmente a través de interacciones con la microbiota gastrointestinal (GI).
El desarrollo de la microbiota gastrointestinal en los primeros meses de vida coincide con un período crítico de la estructura intestinal y la maduración del sistema inmunitario.